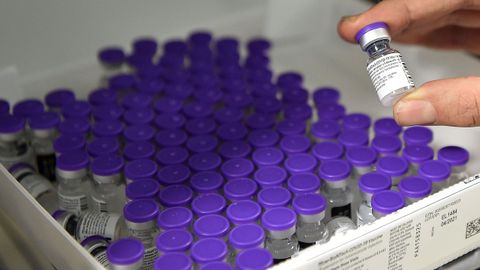
«Faltan otras vacunas autorizadas y nosotros tendremos que llenar el vacío con la nuestra», ha asegurado el CEO alemán | La OMS ha validado el uso de emergencia de la vacuna de Pfizer
01 ene 2021 . Actualizado a las 18:53 h.La empresa alemana BioNTech, que desarrolló la primera vacuna contra el coronavirus junto con el consorcio estadounidense Pfizer, aumentará la producción para cubrir las necesidades de los países de la UE, en los que hay de momento cierta escasez para lograr inmunizar a toda la población.
En una entrevista con la revista Der Spiegel el CEO de BioNTech atribuyó la escasez actual en parte a la política de compras de la UE en la que el proceso ha sido mas lento que en otras partes del mundo.
«El proceso en Europa no fue tan rápido y directo como en otros países y eso se debe también a que la UE no autorizó los pedidos directamente sino que los países miembros también tenían voz. En una negociación en la que se requiere un anuncio claro eso es algo que puede costar tiempo», dijo Sahin.
«Existía el supuesto de vendrían muchas otras empresas con vacunas. Al parecer existía la impresión de que habría suficiente y que las cosas no serían graves, eso me sorprendió», agregó.
Eso ha llevado, según Sahin, a que haya escasez porque «faltan otras vacunas autorizadas y nosotros tendremos que llenar el vacío con nuestra vacuna».
La entrevista de Sahin se produce en momentos en que Alemania se ha criticado por la lentitud de la campaña de vacunación que empezó el 27 de diciembre.
La directora médica de BioNTech, Ózlem Türeci, dijo, por su parte, que la idea de crear un especie de cesto con vacunas de diversos productores era en principio acertada pero llegó el momento en que se vio que muchos no podrían cumplir al tiempo con las órdenes.
El aumento de la producción, según Türeci, no es fácil ya que «no es que haya en todo el mundo fábricas especializadas que puedan producir de la noche a la mañana con la calidad necesaria.
BioNTech ha encargado ya a cinco fabricantes en Europa de la producción de la vacuna y está negociando nuevos contratos.
Sahin tiene esperanzas en el efecto que tendrá una nueva fábrica en Marburg (centro de Alemania) que puede hacer posible que en el primer semestre se produzcan 250 millones de dosis.
La OMS valida el uso de emergencia de la vacuna de Pfizer
La Organización Mundial de la Salud (OMS) ha validado este jueves la vacuna Comirnaty COVID-19 mRNA para uso de emergencia, lo que convierte a esta vacuna producida por el fabricante Pfizer/BioNTech en la primera en recibir este tipo de homologación desde que comenzó el brote del virus nuevo coronavirus en China hace un año.
Según ha explicado la agencia de la ONU, este paso abre la puerta a que los países afectados por la pandemia aceleren sus propios procesos de aprobación regulatoria para importar y administrar la vacuna, además de permitir a UNICEF y a la Organización Panamericana de la Salud adquirir la vacuna para distribuirla a los países que la necesiten.
«Este es un paso muy positivo para garantizar el acceso global a las vacunas contra la COVID-19», ha resaltado la doctora Mariangela Simao, subdirectora general de la OMS para el Acceso a Medicamentos y Productos Sanitarios, si bien ha resaltado «la necesidad de un esfuerzo mundial aún mayor para lograr un suministro de vacunas suficiente para satisfacer las necesidades de las poblaciones prioritarias en todas partes».
Simao ha asegurado que la OMS «trabaja día y noche para evaluar otras vacunas que han alcanzado estándares de seguridad y eficacia». En este sentido, ha animado «a más desarrolladores a que se presenten para revisión y evaluación», incidiendo en que esto es «de vital importancia» para asegurar el suministro necesario para todos los países del mundo y «detener la pandemia».
Los expertos en reglamentación de medicamentos de todo el mundo, convocados por la OMS, y los propios equipos de la organización han revisado los datos sobre la seguridad, eficacia y calidad de la vacuna Pfizer/BioNTech como parte de un análisis de riesgo versus beneficio.
La revisión ha permitido determinar que la vacuna cumple con los criterios imprescindibles de seguridad y eficacia establecidos y que los beneficios de usarla para abordar el covid-19 compensan los riesgos potenciales.
Protocolos
Por otra parte, la OMS ha indicado que también se está llevando a cabo una revisión de los protocolos para la vacuna. Así, está previsto que el Grupo Asesor Estratégico de Expertos en Inmunización de la OMS se reúna el próximo 5 de enero para formular las políticas y recomendaciones específicas para el uso de este producto en las poblaciones, basándose en las recomendaciones de priorización publicadas en septiembre de 2020.
La vacuna Comirnaty requiere almacenamiento mediante una cadena de ultrafrío por lo que debe almacenarse entre -60° y -90° grados centígrados, lo cual complica la vacunación en entornos donde el equipo de la cadena de ultra frío puede no estar disponible o no ser accesible de manera confiable. Por ello, la OMS está trabajando para ayudar a los países a evaluar sus planes de entrega y prepararse para su uso cuando sea posible.