
Las consecuencias de los golpes en la cabeza de forma repetida vienen siendo objeto de estudio desde hace alrededor de un siglo. Ya en el año 1928 el médico estadounidense Harrison Stanford Martland (el mismo que identificó que el radio era la causa del cáncer y la muerte entre las pintoras de esferas de relojes que, sí, antiguamente se pintaban con este elemento para que fueran luminiscentes) publicó un estudio en el que describía un síndrome que denominó «punch drunk» (algo así como «borracho de golpes») que afectaba sobre todo a los boxeadores y que causaba síntomas como temblores, problemas de memoria y deterioro mental. Este síndrome lo relacionó claramente con los golpes repetidos en la cabeza que estos deportistas sufrían. Este se considera el primer estudio serio que asocia impactos repetidos con daño neurológico.
Durante las siguientes décadas del siglo XX este síndrome se sigue estudiando en boxeadores y el término original de «punch drunk» evoluciona a «dementia pugilistia» («demencia pugilística»), pues durante estos años de investigación se confirma que es una enfermedad progresiva similar a otros tipos de demencia (el término demencia se utiliza para describir una variedad de afecciones neurológicas que afectan al cerebro y que empeoran con el tiempo, es decir, que son degenerativas). Sin embargo, las investigaciones quedaron muy limitadas al contexto del boxeo y no se llegó a generalizar a otros deportes.
Fue a principios del siglo XXI, concretamente en el año 2002, cuando este tema adquiere una dimensión global. Es en este año cuando Bennet Omalu, médico forense nigeriano-estadounidense afincado en Pittsburgh (Pensilvania, Estados Unidos), acuña el nombre por el que hoy en día conocemos a esta patología, la Encefalopatía Traumática Crónica (CTE). Este médico realizó la autopsia de Mike Webster, un famoso jugador de los Pittsburgh Steelers, el equipo local de la National Football League (la famosa NFL, lo que en Europa se conoce como fútbol americano), y durante la misma se paró a examinar su cerebro. Tras un análisis minucioso, se dio cuenta de que éste tenía ciertas anomalías e identifico un patrón de daño específico que denominó encefalopatía traumática crónica (CTE).
Su investigación en aquella época fue muy polémica porque una patología que hasta entonces solo se asociaba a los boxeadores, había sido detectada en un deporte diferente, uno que es seguido por millones de personas en Estados Unidos. Esto le acarreó muchos problemas y un conflicto muy sonado con la NFL que sirvió para dar visibilidad a la CTE. Finalmente, tras varios casos más, la NFL aceptó las conclusiones del estudio y tomó algunas medidas de seguridad para paliar la incidencia de la patología entre los jugadores. La historia de Bennet Omalu y su investigación de la CTE se relata en la película La verdad duele («Concussion» es su nombre original en inglés), con Will Smith protagonizando a Bennet Omalu. En ella se narra la lucha de este médico contra la NFL, que tenía la intención de desacreditar su investigación sobre la CTE, y las consecuencias de este enfrentamiento para su vida personal y profesional.
Desde entonces, el estudio y el seguimiento de esta patología ha sido mucho más intenso. Sin embargo, los científicos seguían sin comprender el mecanismo exacto por el que los años recibiendo golpes en la cabeza al practicar ciertos deportes de contacto pueden traducirse en una grave pérdida de memoria y demencia a largo plazo. Y la clave está en la llamada barrera hematoencefálica.
La barrera hematoencefálica es una estructura altamente selectiva que protege al sistema nervioso central al regular el paso de sustancias entre la sangre y el tejido cerebral. Esta barrera es crucial para mantener la homeostasis, que es la capacidad del cerebro para mantener un equilibrio interno estable a pesar de cambios en el entorno o en el propio organismo. El cerebro necesita condiciones muy precisas para trabajar bien. Son indispensables determinados niveles y valores de oxígeno y glucosa (que son el combustible básico de las neuronas), de temperatura, de equilibrio de iones (sodio, potasio, calcio…), de acidez, de flujo sanguíneo o de concentración de neurotransmisores. La barrera hematoencefálica es la encargada de proteger el cerebro de sustancias nocivas mientras permite el paso selectivo de nutrientes esenciales y elimina productos de desecho.
Es importante entender que la barrera hematoencefálica (BHE) es parte de los capilares del cerebro, es decir, no está «alrededor» como una funda externa, sino que son los propios capilares que en el cerebro tienen esta modificación. La sangre entra al cerebro por arterias «normales» (como las carótidas o las vertebrales) que se van ramificando, formando primero las arteriolas y después los capilares. Es en estos capilares cerebrales donde aparece la barrera hematoencefálica. Se podría decir que son unos capilares «especiales» que solo están en el cerebro y cuyas paredes constituyen la barrera hematoencefálica.
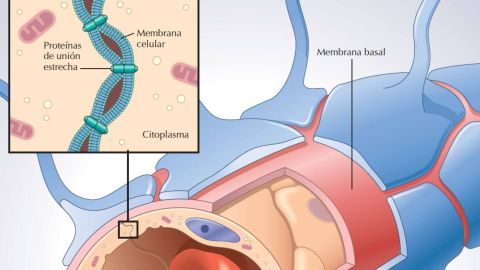
Sus funciones tan especializadas se dan gracias a su particular morfología. Está compuesta por varios componentes que trabajan en conjunto para regular el transporte de sustancias (ver imagen 1). Por un lado, tenemos las células endoteliales del capilar, que son la base estructural de la barrera, las paredes que rodean la luz del capilar (el agujero por el que circula la sangre). Estas células están unidas por lo que se conoce como uniones estrechas, que limitan el intercambio de sustancias entre las células (el intercambio de sustancias sin pasar por dentro de las células se denomina paracelular). Las uniones estrechas juegan un papel fundamental, pues evitan «filtraciones» entre las células sellando el espacio libre entre ellas. Esto obliga a que toda sustancia tenga que pasar a través de las células (transporte o intercambio de sustancias vía transcelular) haciendo el intercambio de sustancias altamente selectivo (se puede filtrar mucho mejor lo que llega al cerebro si la sustancia pasa por dentro de las células que si lo hace por fuera de ellas). Rodeando a las células endoteliales tenemos la membrana basal que proporciona soporte estructural y actúa como una barrera física adicional. Los astrocitos también juegan un papel fundamental. No forman la barrera directamente, pero son esenciales para que funcione bien. Los astrocitos son un tipo de células de soporte del sistema nervioso con forma de estrella, llamadas glía, que no son neuronas, pero cumplen funciones imprescindibles para que las neuronas funcionen bien. De hecho, se encargan de la nutrición de las neuronas, de la regulación del entorno químico (iones, neurotransmisores), participan en la reparación del tejido y contribuyen a la regulación del flujo sanguíneo local. Por otro lado, los astrocitos tienen unas prolongaciones llamadas pies perivasculares que recubren externamente los capilares cerebrales y que inducen y mantienen las uniones estrechas del endotelio, regulan el paso de sustancias y conectan la actividad neuronal con el flujo sanguíneo. Finalmente, hay otro tipo de células llamadas pericitos (no aparecen en la imagen 1) que son células que están incrustadas en la membrana basal y que ayudan a estabilizar la barrera y participan en la regulación del flujo sanguíneo cerebral.
Como decimos, la función principal de la barrera hematoencefálica es mantener la homeostasis del cerebro y para ello evita el paso de microorganismos, toxinas y compuestos potencialmente dañinos al tejido cerebral, controla la entrada de nutrientes, como glucosa y aminoácidos, y la salida de desechos metabólicos y actúa como una barrera significativa en la administración de tratamientos farmacológicos dirigidos al cerebro (con el inconveniente de que, en muchas ocasiones, limita su eficacia en el tratamiento de algunas enfermedades al no poder superar la barrera los principios activos del fármaco). Todo ello lo logra debido a que su permeabilidad está estrictamente regulada. La pérdida de su impermeabilidad o, lo que es lo mismo, su capacidad de «filtrado» significaría que sustancias no deseadas para el cerebro comenzarían a penetrar en él con consecuencias, en la mayoría de los casos, perjudiciales.
Desde finales del siglo XX se sabe que la pérdida de la impermeabilidad de la barrera hematoencefálica está relacionada con cambios en el sistema inmunitario y el deterioro cognitivo. Por otro lado, también se ha observado que los traumatismos craneoencefálicos causan daño en esta barrera ocasionando un aumento de su permeabilidad. A pesar de esto, la CTE, cuyo factor principal son los golpes repetidos en la cabeza (no se han descrito casos claros de CTE sin historia de traumatismos repetidos), no había sido relacionada con alteraciones de la barrera hematoencefálica. Sin embargo, esta situación ha cambiado muy recientemente. Un nuevo estudio de mediados de marzo de este mismo año revela que la barrera hematoencefálica puede estar dañada y volverse permeable incluso varios años después de que un deportista sometido a impactos repetidos en la cabeza se retire. Esta pérdida de impermeabilidad de la barrera hematoencefálica persistente parece ser la desencadenante de una respuesta inmunitaria duradera que está estrechamente vinculada al deterioro cognitivo.
Lo que ocurre es que cuando hay un daño en la barrera hematoencefálica, sustancias que no deberían penetrarla, comienza a hacerlo y, por lo tanto, pasan a estar en contacto con el cerebro. La mayoría de estas sustancias suelen ser proteínas plasmáticas (proteínas como la albúmina, la globulina o el fibrinógeno que están disueltas en plasma sanguíneo), toxinas y metabolitos que no deberían estar ahí. Una vez dentro, el sistema inmune reconoce a todas estas sustancias como algo «extraño» y activa el mecanismo de defensa. En el cerebro tenemos las microglías, que son las células inmunitarias propias del cerebro. Forman parte de la glía (como los astrocitos), pero su función es principalmente defensiva. Estás se activan contra la «amenaza» y se empiezan a liberar citoquinas (pequeñas proteínas de señalización que utilizan las células, sobre todo las del sistema inmunitario, para comunicarse entre sí) que generan una respuesta inflamatoria. Esta inflamación esta ocasionada por sustancias como la histamina, las prostaglandinas o los radicales libres, que ayudan a reparar el daño. En el cerebro, estas sustancias están más controladas y son producidas principalmente por la microglía y los astrocitos. Además, como la barrera está dañada, pueden llegar más células inmunes desde la sangre. Esto produce una inflamación en la zona afectada que se retroalimenta, a más inflamación, más señales de las citoquinas, llegada de más sustancias para reparar el daño (aquí reconocidas como «extrañas») por la pared dañada y más inflamación. Una inflamación severa en cualquier parte del cuerpo no es un problema muy grave, pero en el cerebro tenemos un equilibrio muy delicado. El tejido cerebral no tolera bien la respuesta inflamatoria, pues las neuronas son muy sensibles y además son muy poco regenerativas. Lo que puede ocurrir es que el entorno neuronal se altere y se dañen las sinapsis, que son muy delicadas, provocando una disfunción severa. Por lo tanto, lo que en otras partes del cuerpo nos ayuda a combatir el daño, en el cerebro genera estrés oxidativo, daño sináptico e, incluso, muerte neuronal. Es decir, el mecanismo de defensa termina dañando neuronas sanas.
Una de las novedades de este nuevo estudio es como se realizó la toma de datos. Hasta ahora, los investigadores en este tema se encontraban con la dificultad de que para estudiar los efectos a largo plazo de los traumatismos craneales que pueden derivar en algunas enfermedades neurodegenerativas, como la encefalopatía traumática crónica (CTE), solo se podía analizar el tejido neuronal tras la muerte del paciente. Estos estudios post mortem dan mucha información, pero la cuestión de si se podían detectar señales de alerta en deportistas vivos seguía abierta. Por ello, los investigadores decidieron escanear los cerebros de 47 deportistas retirados que habían practicado deportes de contacto con alto riesgo de conmoción cerebral y golpes repetidos en la cabeza, como el rugby y el boxeo, y analizar minuciosamente el estado de la barrera hematoencefálica de sus cerebros. A su vez, también hicieron el mismo examen en un grupo de control formado por personas no deportistas y por deportistas de disciplinas sin contacto.
Las imágenes cerebrales mostraron que las barreras hematoencefálicas de los deportistas de contacto eran significativamente más permeables que las de las personas del grupo de control, a pesar de que los deportistas llevaban retirados una media de 12 años en el momento del estudio, lo que significa que el daño en la barrera hematoencefálica persiste muchos años después de la retirada y el cese de los golpes. Esto constituye la primera prueba de que la barrera hematoencefálica está alterada en personas con probabilidad de tener CTE. Las personas con el daño más extenso en la barrera obtuvieron peores resultados en pruebas de memoria y cognitivas que aquellas con menor grado de permeabilidad.
Al examinar el sistema inmunitario de los deportistas con daño en la barrera y mayor deterioro cognitivo, se comprobó que su sangre contenía una mayor proporción de glóbulos blancos inflamatorios y otros biomarcadores de activación inmunitaria que la de aquellas con daño menos extenso. Esto encaja con la situación de permeabilidad de la barrera que hemos descrito anteriormente.
Este hallazgo sugiere que las imágenes cerebrales capaces de detectar estos vasos sanguíneos permeables podrían servir algún día como herramienta para diagnosticar a personas con alto riesgo de enfermedades cerebrales graves. Los resultados también abren la puerta al desarrollo de tratamientos farmacológicos enfocados en la reparación de la barrera hematoencefálica que sirvan para prevenir este tipo de enfermedades neurodegenerativas.

Comentarios